 Un soir d’automne 1906, 400 convives sont attablés dans la grande salle de banquet du prestigieux établissement Delmonico’s, à New York. Dress code: tout le monde en smoking. Rien que de très ordinaire. Ce qui l’est moins, c’est qu’ils portent tous exactement le même nœud papillon.
Un soir d’automne 1906, 400 convives sont attablés dans la grande salle de banquet du prestigieux établissement Delmonico’s, à New York. Dress code: tout le monde en smoking. Rien que de très ordinaire. Ce qui l’est moins, c’est qu’ils portent tous exactement le même nœud papillon.
Un nœud papillon violet.
À côté de son assiette, chacun a trouvé la copie d’un brevet, qui porte le nom de l’invité d’honneur de la soirée: Sir William Henry Perkin. Un brevet vieux de 50 ans.
 En 1856, William Perkin, pas encore Sir, est le fils d’un menuisier de l’East End londonien. Son père aurait aimé le voir en école d’architecture, mais le jeune Perkin a préféré s’inscrire au tout nouveau Collège Royal de Chimie. L’Angleterre ayant pris beaucoup de retard sur l’Allemagne dans la discipline, c’est un disciple de Liebig et expert en chimie organique, August von Hofmann[1], qui est chargé de l’enseignement.
En 1856, William Perkin, pas encore Sir, est le fils d’un menuisier de l’East End londonien. Son père aurait aimé le voir en école d’architecture, mais le jeune Perkin a préféré s’inscrire au tout nouveau Collège Royal de Chimie. L’Angleterre ayant pris beaucoup de retard sur l’Allemagne dans la discipline, c’est un disciple de Liebig et expert en chimie organique, August von Hofmann[1], qui est chargé de l’enseignement.
2 problèmes de chimie
 Et vers 1850, Londres offre aux apprentis chimistes deux gros sujets de réflexion. Il y a d’abord des déchets: depuis des décennies on distille la houille par millions de tonnes pour en extraire le coke qui sert de combustile, et le gaz (de charbon, donc) qui sert à éclairer la ville. Mais le procédé produit aussi des gaz soufrés (tant pis pour les voisins), de l’eau polluée (hop, dans la Tamise) et du goudron. Noir, puant, visqueux [2]… et inutile ? Après quelques années on a quand même fini par lui trouver quelques usages: imperméabiliser les traverses de chemin de fer, par exemple. Ou des vêtements pour la pluie (le célèbre Mackintosh). Mais on en a des quantités astronomiques… pourrait-on en faire autre chose ?
Et vers 1850, Londres offre aux apprentis chimistes deux gros sujets de réflexion. Il y a d’abord des déchets: depuis des décennies on distille la houille par millions de tonnes pour en extraire le coke qui sert de combustile, et le gaz (de charbon, donc) qui sert à éclairer la ville. Mais le procédé produit aussi des gaz soufrés (tant pis pour les voisins), de l’eau polluée (hop, dans la Tamise) et du goudron. Noir, puant, visqueux [2]… et inutile ? Après quelques années on a quand même fini par lui trouver quelques usages: imperméabiliser les traverses de chemin de fer, par exemple. Ou des vêtements pour la pluie (le célèbre Mackintosh). Mais on en a des quantités astronomiques… pourrait-on en faire autre chose ?
 Et il y a ensuite une maladie: la malaria sévit encore en Angleterre, et fait encore plus de ravages dans l’Inde désormais britannique: 2 millions de morts par an[3]. Dans les années 1820, on a trouvé un bon remède: la quinine. Mais la quinine est rare, et chère: pas d’autre choix que d’importer d’Amérique du sud d’énormes quantités d’écorce de quinquina. Rien que pour l’armée coloniale, la Compagnie des Indes dépense 100 000 livres par an. Si seulement on trouvait un moyen de la fabriquer pour moins cher !
Et il y a ensuite une maladie: la malaria sévit encore en Angleterre, et fait encore plus de ravages dans l’Inde désormais britannique: 2 millions de morts par an[3]. Dans les années 1820, on a trouvé un bon remède: la quinine. Mais la quinine est rare, et chère: pas d’autre choix que d’importer d’Amérique du sud d’énormes quantités d’écorce de quinquina. Rien que pour l’armée coloniale, la Compagnie des Indes dépense 100 000 livres par an. Si seulement on trouvait un moyen de la fabriquer pour moins cher !
Un échec
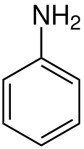
 Et voilà qu’Hofmann a une idée formidable: pourrait-on synthétiser la quinine à partir du goudron de houille ? Ce n’est pas si farfelu que ça: petit à petit, ses prédécesseurs ont déjà identifié plusieurs composants du goudron, et ils se retrouvent souvent dans des plantes exotiques. Ainsi Michael Faraday a isolé une molécule qu’on a appelée benzène, parce qu’on la trouve aussi dans la résine de benjoin (ou storax). Berzelius a baptisé le toluène du nom d’un extrait végétal péruvien (le baume de tolu). Et Hofmann lui-même a démontré que l’aniline, C6H7N, était la même dans le goudron et dans l’indigo (en latin Anila tinctoria). Or en 1854, on a trouvé la formule brute de la quinine: C20H24N2O2… Du carbone, de l’hydrogène, de l’azote et de l’oxygène, il y en a dans le goudron: plus qu’à les recombiner correctement !
Et voilà qu’Hofmann a une idée formidable: pourrait-on synthétiser la quinine à partir du goudron de houille ? Ce n’est pas si farfelu que ça: petit à petit, ses prédécesseurs ont déjà identifié plusieurs composants du goudron, et ils se retrouvent souvent dans des plantes exotiques. Ainsi Michael Faraday a isolé une molécule qu’on a appelée benzène, parce qu’on la trouve aussi dans la résine de benjoin (ou storax). Berzelius a baptisé le toluène du nom d’un extrait végétal péruvien (le baume de tolu). Et Hofmann lui-même a démontré que l’aniline, C6H7N, était la même dans le goudron et dans l’indigo (en latin Anila tinctoria). Or en 1854, on a trouvé la formule brute de la quinine: C20H24N2O2… Du carbone, de l’hydrogène, de l’azote et de l’oxygène, il y en a dans le goudron: plus qu’à les recombiner correctement !
 Sa première idée, ce serait de partir de la naphtylamine. Si on ne regarde que les formules brutes (et Hofmann n’a accès qu’à ça), il faudrait « juste » la combiner avec de l’eau pour en faire de la quinine. Il n’est pas naïf au point de croire qu’il suffira de mélanger les deux, mais il espère un « heureux accident » et met son plus jeune étudiant au travail… avant de partir en vacances. Perkin, installé dans sa petite chambre-laboratoire au-dessus de chez ses parents, s’attelle aux expériences. Il oxyde, il distille, il purifie… et au lieu d’obtenir la quinine incolore il arrive à une poudre rouge. Raté. Il recommence en partant de l’aniline, plus simple. Cette fois le résultat est juste un résidu tout noir: encore un échec.
Sa première idée, ce serait de partir de la naphtylamine. Si on ne regarde que les formules brutes (et Hofmann n’a accès qu’à ça), il faudrait « juste » la combiner avec de l’eau pour en faire de la quinine. Il n’est pas naïf au point de croire qu’il suffira de mélanger les deux, mais il espère un « heureux accident » et met son plus jeune étudiant au travail… avant de partir en vacances. Perkin, installé dans sa petite chambre-laboratoire au-dessus de chez ses parents, s’attelle aux expériences. Il oxyde, il distille, il purifie… et au lieu d’obtenir la quinine incolore il arrive à une poudre rouge. Raté. Il recommence en partant de l’aniline, plus simple. Cette fois le résultat est juste un résidu tout noir: encore un échec.
La chimie inutile
Voulait-il simplement nettoyer son récipient, ou tenter malgré tout de travailler avec ce produit inconnu ? Toujours est-il que Perkin récupère un peu du truc noir, le dissout dans l’alcool… et obtient une magnifique couleur violette. À tout hasard, il y fait tremper un petit morceau de soie… la couleur prend. Mieux, elle semble résister au lavage et à la lumière ! Du coup, à tout hasard il envoie un échantillon à un teinturier. Qui se montre plutôt enthousiaste: la pourpre est la couleur prestigieuse par excellence, mais —comme toutes les teintures naturelles — elle est difficile à produire, difficile à faire tenir sur les tissus, et horriblement chère[4]. Perkin peut-il faire mieux avec son invention ?

Le jeune étudiant (il n’a que 18 ans) hésite mais finit par avouer sa découverte à Hofmann… qui, lui, ne se montre absolument pas intéressé: après tout, c’est la quinine qu’il cherche. Et puis des liquides colorés, tous les chimistes passent leur temps à en obtenir ; aucun n’a jamais songé à les exploiter. Qui plus est pour un usage aussi futile que teindre des vêtements !
La robe de la Reine

Hofmann désapprouve et regrette de perdre un étudiant prometteur, mais Perkin quitte le collège de chimie, dépose le fameux brevet, puis tente de commercialiser l’invention. Il faut trouver un moyen de faire tenir le colorant sur le coton aussi bien que sur la soie. Il faut traiter des tonnes de charbon rien que pour obtenir l’aniline de départ. Et faute d’investisseur, compter sur les économies de son père.  Avec son frère et deux teinturiers motivés, il construit une usine pionnière à tous points de vue: personne n’a jamais fabriqué et manipulé les molécules dérivées du goudron en si grandes quantités. Et personne n’a jamais produit un colorant synthétique ! Il faut un nom à sa teinture: c’est le nom français d’une petite fleur, la mauve, qui va s’imposer (et donner son nom à la molécule: mauvéine). Mais même s’il dispense de broyer des milliers de petits coquillages, le colorant de Perkin reste très cher: 3 fois le prix du platine ! Forcément: pour obtenir 10 g de poudre, il faut 60 kg de charbon. Mais heureusement, avec 10 g de mauve on peut teindre 2 kg de coton !
Avec son frère et deux teinturiers motivés, il construit une usine pionnière à tous points de vue: personne n’a jamais fabriqué et manipulé les molécules dérivées du goudron en si grandes quantités. Et personne n’a jamais produit un colorant synthétique ! Il faut un nom à sa teinture: c’est le nom français d’une petite fleur, la mauve, qui va s’imposer (et donner son nom à la molécule: mauvéine). Mais même s’il dispense de broyer des milliers de petits coquillages, le colorant de Perkin reste très cher: 3 fois le prix du platine ! Forcément: pour obtenir 10 g de poudre, il faut 60 kg de charbon. Mais heureusement, avec 10 g de mauve on peut teindre 2 kg de coton !
Les débuts de la nouvelle manufacture sont compliqués, mais quelques années plus tard c’est le jackpot: et la reine Victoria et l’impératrice Eugénie décident de porter du mauve ! La mode est lancée, le colorant de Perkin envahit l’Europe, et sa fortune est faite. Comme toutes les modes, elle va vite passer… mais celle de nouvelles couleurs plus vives et moins chères, non. En Angleterre, en France, en Allemagne, partout des concurrents apparaissent, se disputent les brevets, et c’est toute une industrie qui se met en branle. Même le distingué professeur Hofmann a fini par changer d’avis: toujours en bidouillant à partir de l’aniline (qu’il a commandée à Perkin !), il arrive à d’autres nuances violettes avec la fuchsine, puis au magenta, puis au rouge de quinoléine. De son côté Perkin obtient un nouveau bleu, un rose, un orange, un vert… L’ère des colorants de synthèse ne fait que commencer [5], et il aura fallu un accident pour la faire jaillir d’une pâte noire, épaisse et malodorante.
Aller plus loin
- Ce billet est basé sur l’histoire de Perkin et de la naissance d’une industrie, racontées dans l’ouvrage [en anglais] de Simon Garfield: Mauve. Et sur les teintures entre beaucoup d’autres choses, il faut évidemment lire la série des « Histoire d’une couleur » (bleu, noir, vert, rouge) de Michel Pastoureau.
- Le parcours de Perkin est une histoire de sérendipité, mais aussi à travers sa relation avec Hofmann, des liens ambigus, voire conflictuels entre recherche fondamentale et appliquée. Voici ce que le chimiste se remémore des conséquences de son choix de carrière:
Pour un scientifique, se mêler de fabrication était vu comme une occupation inférieure. Les chercheurs qui franchissaient cette ligne étaient traités comme des parias, des traîtres à la cause.
On a dit que par mon exemple, j’avais nui à la science, et détourné les esprits des jeunes hommes de la science pure vers la science appliquée ; et il est possible que pendant quelque temps, certains aient été attirés vers la chimie pour des motifs autres que purement scientifiques.
- Et la quinine alors ? Il faudra attendre encore un siècle (1944) pour arriver à la première méthode de synthèse. On a fait des progrès depuis, mais toujours pas trouvé de procédé industriel moins cher que l’extraction de l’écorce. Quant à la mauvéine, elle aussi a posé bien des difficultés aux chimistes: il a fallu attendre 1994 pour avoir une idée exacte de sa structure moléculaire (ou plutôt de ses structures, puisqu’elle est en réalité un mélange). Mais entre-temps, à défaut de traiter la malaria, c’est quand même en manipulant les molécules colorantes et leurs dérivées (et en découvrant leurs propriétés antalgiques ou antibiotiques) qu’on parviendra aux premiers médicaments de synthèse… Hofmann n’était pas si loin du compte !
[1] À ne pas confondre avec le chimiste suisse Albert Hofmann, qui découvrit le LSD. Ni avec Fritz Hofmann, qui fabriqua le premier caoutchouc synthétique. Encore moins avec leur presque homonyme Felix Hoffmann, qui a la fin du siècle synthétisera l’aspirine. Ni avec Friedrich ou Roald du même nom, eux aussi chimistes ! ↑
[2] En anglais coal tar… et donc parfois en français, coltar ! ↑
[3] Aujourd’hui, la malaria touche 200 millions de personnes dans le monde et fait plus d’un demi-million de morts chaque année. ↑
[4] Par exemple, pour obtenir 10 grammes de poudre de carmin de cochenille, il faut broyer plus de 5 000 insectes ! ↑*
[5] Et avec elle les doutes sur leur innocuité: dès les années 1860, l’arsenic et le mercure contenus dans certaines des premières teintures font débat. ↑
Pingback: La plus vieille question du monde | La Forêt des Sciences